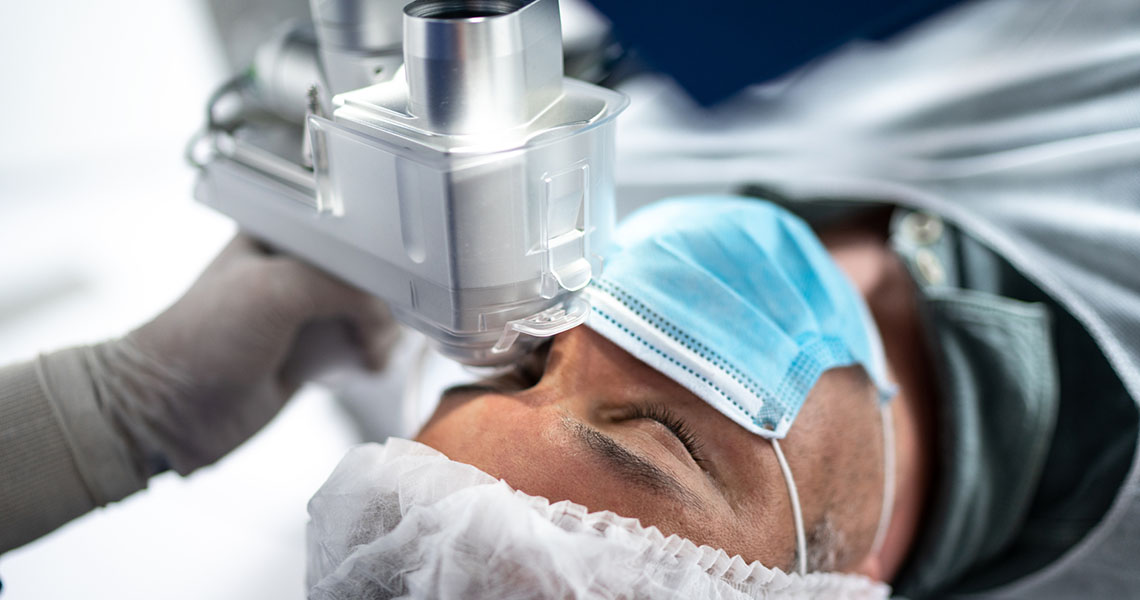
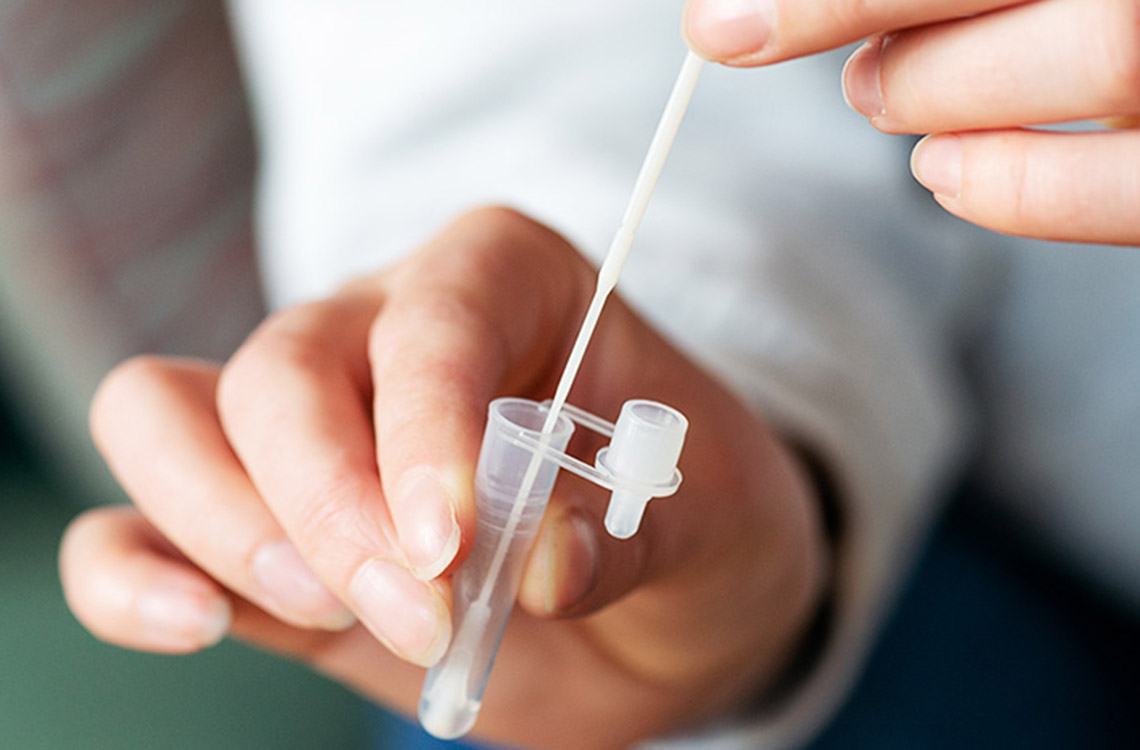
Lääkinnällisiin laitteisiin kuuluu kirjava joukko tarvikkeita, välineitä ja ohjelmistoja, joiden tehtävänä on diagnosoida, ehkäistä tai hoitaa sairauksia ja vammoja. Tarkastaja Minna Kymäläinen käsittelee ja valvoo Fimeassa niihin liittyviä kliinisiä tutkimuksia.
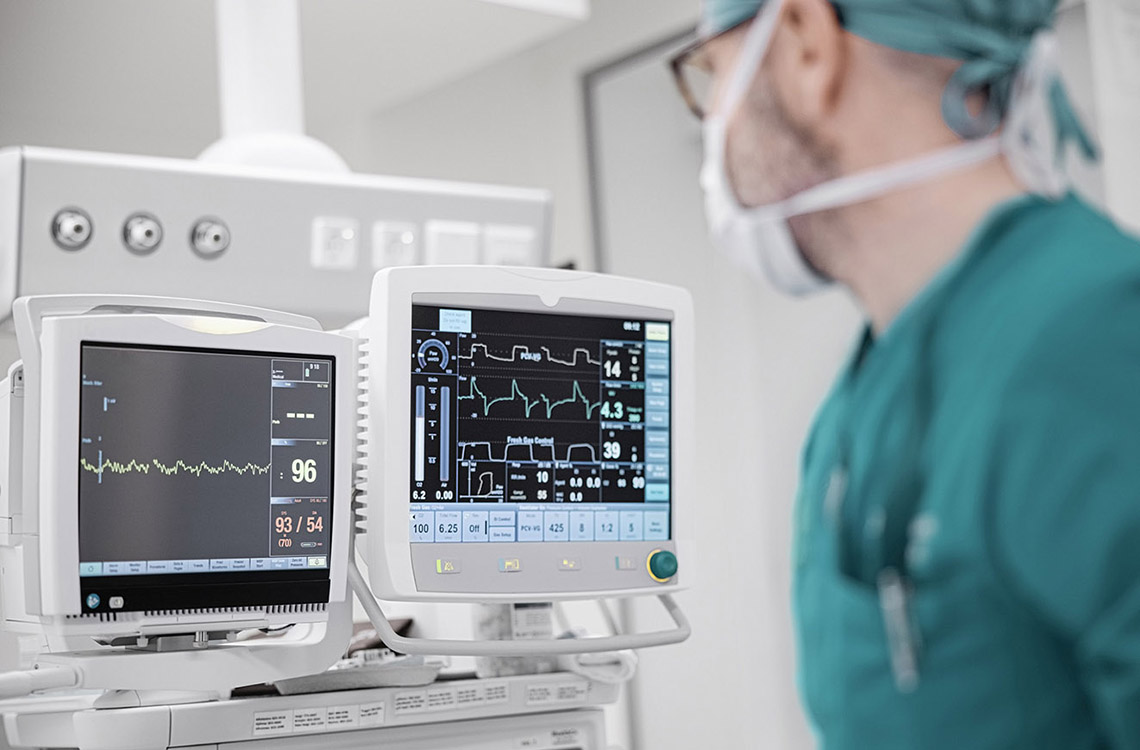
Lääkinnällinen laite tuo usein ensimmäisenä mieleen terveydenhuollossa käytettävän elektronisen laitteen, kuten röntgenlaitteen tai hengityskoneen. Termillä tarkoitetaan kuitenkin kaikenlaisia tarvikkeita, välineitä ja ohjelmistoja, joiden tehtävänä on diagnosoida, ehkäistä tai hoitaa sairauksia ja vammoja.
– Kotona käytettävät verenpainemittarit ovat lääkinnällisiä laitteita, samoin raskaustestit, silmälasit, laastarit ja jopa lihaskipuihin käytettävät kylmägeelit, kertoo tarkastaja Minna Kymäläinen Fimeasta.
Tuotteen käyttötarkoitus ja vaikutusmekanismi määrittävät, onko tuote lääkinnällinen laite vai jokin muu, esimerkiksi lääke tai kosmeettinen valmiste.
Keskeinen ero lääkkeen ja lääkinnällisen laitteen välillä on, että lääkkeen vaikutus elimistössä on farmakologinen, metabolinen tai immunologinen, mutta laitteella tällaista vaikutusta ei ole. Kosmetiikka ja hygieniatuotteet eivät puolestaan lievitä tai hoida mitään.
– Joskus rajanveto on todella haastavaa. Meillä on markkinoilla esimerkiksi raskauden ehkäisyyn hormonikierukka, joka on lääke, mutta myös kuparikierukka, joka on laite, Kymäläinen vertaa.
Jotta lääkinnällisen laitteen voi tuoda markkinoille, valmistajan tulee osoittaa, että tuote on turvallinen ja suorituskykyinen siinä ympäristössä, jossa sitä on tarkoitus käyttää. Kuluttaja tunnistaa tällaisen tuotteen CE-merkistä.
Yli puoli miljoonaa laitetta
Fimea valvoo lääkinnällisiä laitteita ja alan toimijoita Suomessa. Valvonta kattaa esimerkiksi laitteiden markkinoinnin, vaaratilanneilmoitukset sekä kliiniset eli ihmisillä tehtävät tutkimukset.
Lääkinnällisten laitteiden valvonnan parissa työskentelee Fimeassa 18 henkilöä. Minna Kymäläinen keskittyy neljän kollegansa kanssa kliinisten laitetutkimusten käsittelyyn ja valvontaan.
– Työtä on paljon, sillä Euroopan laajuisesti markkinoilla on yli puoli miljoonaa lääkinnällistä laitetta. Meille tuli viime vuonna yli 4 700 vaaratilanneilmoitusta ja reilut 50 tutkimusilmoitusta, hän kertoo.
Jos jostakin laitteesta tulee paljon vaaratilanneilmoituksia, Fimeassa selvitetään, onko vika kyseisessä laitteessa, sen käytössä, koulutuksessa tai ohjeistuksessa.
Valvontaa toteutetaan esimerkiksi tekemällä tarkastuksia toimijoiden yksiköihin. Jos jostakin laitteesta tulee paljon vaaratilanneilmoituksia, Fimeassa selvitetään, onko vika kyseisessä laitteessa, sen käytössä, koulutuksessa tai ohjeistuksessa.
– Viestiä erilaisista ongelmista tulee myös kilpailijoilta, sairaaloista ja kuluttajilta. Lisäksi seuraamme alan lehdistä ja muiden maiden valvontaviranomaisilta, mitä maailmalla tapahtuu.
Kymäläinen käsittelee kliinisten tutkimusten hakemuksia, pyytää tarvittaessa toimijoilta lisäselvityksiä ja tekee lupapäätöksiä. Lisäksi hän valvoo, että tutkimukset suoritetaan hakemusten mukaisesti, ja opastaa tutkijoita lainsäädännön soveltamisessa.
– Kun saan eteeni uuden tutkimuksen, olen todella innoissani! Meillä on lukematon määrä hyviä tutkimusryhmiä, loistavia akateemisia tutkijoita ja pieniä startup-yrityksiä, joilla on valtavasti osaamista. Olen aitiopaikalla näkemässä, mitä kaikkea kiinnostavaa alalla tehdään, Kymäläinen sanoo hymyillen.
Uusi asetus tiukensi vaatimuksia
Aiemmin lääkinnällisten laitteiden valvonnasta vastasi Suomessa Valvira, mutta se siirtyi Fimean vastuulle vuoden 2021 alusta. Myös lääkinnällisiä laitteita koskeva lainsäädäntö muuttui, kun uusi EU-asetus tuli voimaan keväällä 2021.
Kymäläisen mukaan uusi asetus muutti kliinisten laitetutkimusten vaatimuksia suuresti.
– Tutkijoilta vaaditaan etukäteen paljon enemmän selvityksiä siitä, millainen tutkimus on tekeillä. Myös käsittelyajat muuttuivat tiukemmiksi sekä viranomaisille että ilmoittajille.
Lääkinnälliset laitteet luokitellaan asetuksessa riskiluokkiin I, IIa, IIb ja III sen mukaan, mikä on tuotteen käyttötarkoitus ja millaisia riskejä sen käyttöön liittyy. Mitä korkeampi riskiluokka on, sitä enemmän tuotteelta vaaditaan näyttöä suorituskyvystä ja turvallisuudesta.
– Kolmosluokkaan kuuluu esimerkiksi implantoitavia laitteita, kuten sydänläppiä ja keinoniveliä. Niille on aina tehtävä kliininen tutkimus, ennen kuin tuotteen voi tuoda markkinoille. Muille lääkinnällisille laitteille tutkimukset ovat vapaaehtoisia, Kymäläinen kertoo.
Aiemmin viranomaiset vain ilmoittivat toimijalle, kun tutkimusilmoitus oli käsitelty, mutta nyt asiasta annetaan valituskelpoinen päätös. Lisäksi asetuksessa säädettiin viranomaiselle velvollisuus tehdä tarkastuksia tutkimuspaikkaan.
Asetus mahdollistaa myös sen, että eurooppalaisten monikeskustutkimusten lupahakemukset voidaan tulevaisuudessa käsitellä koordinoidusti yhdessä jäsenmaassa. Kymäläisen mukaan tämä vähentäisi sekä hakijoiden että viranomaisten työtaakkaa.

Ei vain valvoja, vaan mahdollistaja
Suuri osa Minna Kymäläisen työajasta kuluu neuvonnan ja ohjauksen parissa. Uuteen asetukseen liittyviä kysymyksiä on toimijoilla paljon.
– Sama tutkija saattaa soittaa kolme tai neljäkin kertaa ja kysyä, mitä asetuksen vaatimuksilla missäkin kohtaa tarkoitetaan, Kymäläinen kertoo.
Asetuksen mukaan kliinisen tutkimuksen tarkoituksena on varmistaa laitteen suorituskyky, turvallisuus tai molemmat sen tavanomaisessa käyttöympäristössä. Tutkimukset tulee suunnitella ja toteuttaa siten, että osallistujien oikeudet ja hyvinvointi on turvattu. Saatujen kliinisten tietojen tulee olla tieteellisesti päteviä ja luotettavia.
Kymäläinen ei koe olevansa vain tutkimusten valvoja, vaan myös mahdollistaja.
"Toki joskus myös jankutan asetuksen vaatimuksista. Silloin kannattaa muistaa, että viranomainen ei tee sitä kiusallaan, vaan koska hänen on pakko."
– Toki joskus myös jankutan asetuksen vaatimuksista. Silloin kannattaa muistaa, että viranomainen ei tee sitä kiusallaan, vaan koska hänen on pakko, hän huomauttaa.
Fimeassa Kymäläinen on viihtynyt hyvin. Hän kokee, että tässä työyhteisössä on helppo tehdä töitä.
– Minulla on onni tehdä töitä ihmisten kanssa, jotka ajattelevat hyvin samankaltaisesti. Lähellä on aina ihmisiä, joilta voin kysyä apua, hän kiittelee.
Tehtävän takana
Kuka?
Minna Kymäläinen
Mikä on tehtäväsi Fimeassa?
Työskentelen tarkastajana lääkinnällisten laitteiden valvonnassa, jossa keskityn kliinisten tutkimusten käsittelyyn ja valvontaan. Lisäksi tehtäviini kuuluu elinsiirtolupien käsittely ja niihin liittyvä neuvonta.
Mikä on koulutustaustasi?
Olen koulutukseltani erikoissairaanhoitaja. Valmistuin sairaanhoitajaksi vuonna 1988 ja erikoistuin anestesia- ja tehohoitoon vuonna 1992.
Aiempi työurasi ennen Fimeaa?
Valmistumiseni jälkeen työskentelin anestesiasairaanhoitajana Etelä-Karjalan keskussairaalassa sekä HUSissa Meilahden sairaalassa. Se jälkeen siirryin teollisuuteen tutkimuksen ja tuotekehityksen pariin. Työskentelin GE Healthcare -yhtiössä, jossa olin mukana tutkimassa muun muassa unen syvyyden mittausta.
Miksi tulit Fimeaan töihin?
Ajattelin, että voisin kokeilla vielä kolmatta näkökulmaa lääkinnällisten laitteiden maailmaan. Aloitin Lääkelaitoksessa vuonna 2009, eli samana vuonna, kun Lääkelaitoksesta tuli Fimea ja Valvira. Laitepuoli sijoitettiin Valviraan, jonne minäkin siirryin. Fimeaan palasin vuoden 2021 alussa, kun lääkinnällisten laitteiden valvonta siirtyi tänne.
Mikä yllätti Fimeassa?
Ihmisten laaja asiantuntemus on yllättänyt. Oli kyse sitten lääkkeistä, huumausaineista tai vaikkapa kudosvalmisteista, täältä löytyy valtavasti osaamista ja tietotaitoa aiheesta.
Tähtihetki työssä Fimeassa?
Mieleen tulee kaksi tähtihetkeä. Toinen oli Lääkinnällisillä laitteilla tehtävät kliiniset tutkimukset -määräyksen valmistuminen viime vuoden keväällä, toinen elinsiirtotoiminnan kymmenvuotissuunnitelman julkaisu viime vuoden lopulla. Molempien taustalla oli paljon työtä.
Paras tapa nollata työasiat vapaa-ajalla?
Rakastan kulttuuririentoja ja kirjojen lukemista. Minulta saa aina teatterivinkit koko porukalle! Olen myös innokas penkkiurheilija ja osallistun vapaaehtoisena erilaisiin urheilukisoihin. Olin mukana esimerkiksi jääkiekon MM-kisojen ensiapujoukoissa keväällä 2022.
Lääkinnällisten laitteiden valvonta ja kliiniset tutkimukset
- Fimea valvoo lääkinnällisten laitteiden vaatimustenmukaisuutta ja alan toimijoita Suomessa.
- Lisäksi Fimea valvoo muun muassa lääkinnällisten laitteiden markkinointia ja käsittelee niihin liittyviä vaaratilanneilmoituksia.
- Valvonta tapahtuu yhteistyössä muiden EU:n viranomaisten kanssa.
- Lääkinnällisten laitteiden kliinisten tutkimusten tarkoituksena on varmistaa laitteen suorituskyky, turvallisuus tai molemmat sen tavanomaisessa käyttöympäristössä.
- Tutkimuksissa osallistujien oikeudet ja hyvinvointi pitää olla turvattu.
- Tutkimuksissa saatujen kliinisten tietojen tulee olla tieteellisesti päteviä ja luotettavia.