Tarkentunut ja selkiytynyt lainsäädäntö helpottaa viranomaisen ja toimijoiden työtä rajanvetotilanteissa. Kuluttajalle ja ammattilaiselle oleellisinta on käyttää laitetta ohjeiden mukaan valmistajan määrittelemään käyttötarkoitukseen.
Keväällä 2021 uudistuneen lääkinnällisten laitteiden asetuksen soveltamisalaa, määritelmiä ja luokituksia on selkeytetty. Samalla tarkentui asetuksen soveltaminen rajanvetotilanteissa ja yhdistelmätuotteiden kohdalla.
Tuoterajanvetoa joudutaan tekemään esimerkiksi silloin, kun liikutaan lääkkeiden, ihmisperäisten kudostuotteiden, elävien mikrobien, kosmetiikan tai biosidivalmisteiden ja laitteiden rajapinnoilla.
Aiemmassa sääntelyssä oli rajanvetotilanteisiin liittyvää tulkinnanvaraa, joka on vähentynyt lainsäädäntöuudistuksen myötä. Esimerkiksi elävät siirteet, kudokset ja solut eivät ole enää nykyisen laiteasetuksen soveltamisalaa.
Rajanveto vaikuttaa sovellettavaan lainsäädäntöön
Mikään sairaus tai tuoteryhmä ei yksinään määrittele tuotetta lääkinnälliseksi laitteeksi. Valmistajan määrittelemä käyttötarkoitus ja vaikutusmekanismi ovat keskeisiä tekijöitä, kun arvioidaan, onko tuote lääkinnällinen laite vai joku muu tuote, esimerkiksi lääke tai kosmeettinen valmiste. Samaa vaivaa voidaan hoitaa esimerkiksi lääkkeellä tai laitteella. Sovellettavan lainsäädännön kannalta kyseessä on joko lääke tai lääkinnällinen laite.
Yhdistelmätuotteeseen liittyy aina vaatimuksia molempien osien sääntelystä. Esimerkiksi lääkelaiteyhdistelmässä, joita ovat esimerkiksi lääkevalmisteiden esitäytetyt ruiskut, on huomioitava sekä lääke- että laitelainsäädäntö.
Lääkinnällisten laitteiden asetuksessa (artikla 117) kuvataan vaatimukset, jotka koskevat lääkkeeksi luokitellun yhdistelmätuotteen laiteosaa. Lisäksi asetuksessa on kuvattu erityiset lisämenettelyt, joita sovelletaan lääkeainetta sisältäviin laitteisiin. Euroopan lääkevirasto (EMA) on lisäksi julkaissut verkkosivuillaan yhdistelmätuotteisiin liittyvää lisäohjeistusta.
Tuoteluokitteluun ja luokitussääntöjen soveltamiseen on saatavilla tuore lääkinnällisten laitteiden koordinaatioryhmän ohjeistus (MDCG 2021-24, pdf), joka löytyy Euroopan komission verkkosivuilta.
Mihin käyttötarkoitukseen ja miten?
Luokittelu ja rajanveto on viranomaisen ja valmistajan välistä toimintaa. Kuluttajalle tai ammattimaiselle käyttäjälle oleellisinta on ymmärtää, mihin tarkoitukseen ja miten hän valittua tuotetta käyttää, on kyse sitten laitteesta, lääkkeestä tai näiden yhdistelmästä.
Lääkinnällinen laite on valmistajan lääketieteelliseen käyttötarkoitukseen tarkoittama ja riskiluokittelema tuote, jonka valmistaja CE-merkitsee lääkinnälliseksi laitteeksi. CE-merkinnällä valmistaja osoittaa, että laite täyttää lainsäädännössä asetetut vaatimukset. Osasta laitteista löytyy entiseen tapaan myös ilmoitetun laitoksen numero, kun arviointilaitos on osallistunut vaatimustenmukaisuuden arviointiin.
Uudistuneen lainsäädännön myötä CE-merkinnän lisäksi käyttäjälle pitää kertoa, että kyseessä on lääkinnällinen laite. Tämän saa ilmaista käyttöohjeessa ja pakkausmerkinnöissä tekstimuotoisesti tai MD-kuvatunnuksella (kuva 1). Kuvatunnus voi helpottaa lääkinnällisen laitteen tunnistamista ja erottamista muista tuotteista esimerkiksi apteekeissa ja verkkomarkkinoinnissa.
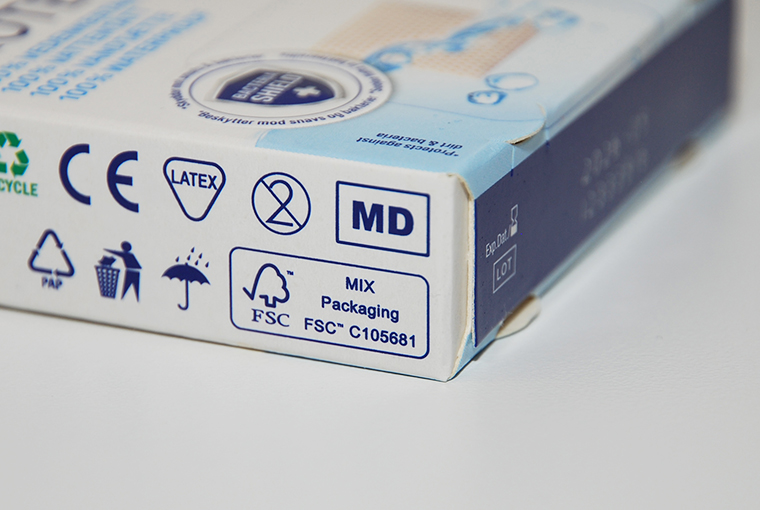
Kuva 1. MD-kuvatunnus lääkinnällisen laitteen pakkauksessa. © Fimea
Viranomaisyhteistyö kansallista ja EU-tasoista
Viranomaiset tekevät tuoteluokittelun, rajanveto- ja yhdistelmätuotteiden osalta tiivistä yhteistyötä kansallisesti ja EU-tasolla. Lisäksi viranomaiset neuvovat valmistajia, maahantuojia, jakelijoita ja ammattimaisia käyttäjiä aihepiiriä koskevissa kysymyksissä.
Uuden lääkinnällisten laitteiden asetuksen vaatimukset ovat entistä tiukemmat, mutta aiempaa selkeämmät. Lääkinnällisten laitteiden sääntelyasemasta ja tuoteluokituksesta päättävät komissio ja kansalliset viranomaiset työnjakonsa mukaisesti. Silti yhteiselle tulkinnalle ja vuoropuhelulle on edelleen tarvetta yhdessä kaikkien toimijoiden kanssa.
Mikä on lääkinnällinen laite?
Laitteella on laitelainsäädännössä määritelty lääketieteellinen käyttötarkoitus.
Laitetta käytetään ihmisillä (ei eläimillä).
Pääasiallista aiottua vaikutusta ei saavuteta farmakologisin, immunologisin tai metabolisin keinoin, mutta toimintaa voidaan tällaisilla keinoilla edistää.
Laite on CE-merkitty lääkinnälliseksi laitteeksi.
Mikä on lääke?
Lääkkeellä tarkoitetaan valmistetta tai ainetta, jonka tarkoituksena on sisäisesti tai ulkoisesti käytettynä parantaa, lievittää tai ehkäistä sairautta tai sen oireita ihmisessä tai eläimessä.
Lääkkeeksi katsotaan myös sisäisesti tai ulkoisesti käytettävä aine tai aineiden yhdistelmä, jota voidaan käyttää ihmisen tai eläimen elintoimintojen palauttamiseksi, korjaamiseksi tai muuttamiseksi farmakologisen, immunologisen tai metabolisen vaikutuksen avulla taikka terveydentilan tai sairauden syyn selvittämiseksi.
Lääkkeissä ei ole CE-merkintää.
Säädöksiä ja lisätietoa
Lääkinnällisten laitteiden asetus (Euroopan parlamentin ja neuvoston asetus (EU) 2017/745, EUR-Lex)
Laki lääkinnällisistä laitteista 719/2021 (Finlex.fi)