Signaaleja rokotteiden mahdollisista haittavaikutuksista saadaan useista eri lähteistä. Valtakunnallisten terveysrekisterien tietojen avulla voidaan selvittää tällaiseen haittasignaaliin liittyvää syy-seuraussuhdetta. Laajat koko väestön kattavat tutkimusaineistot mahdollistavat tutkimustulosten yleistettävyyden ja mahdollistavat usein harvinaistenkin epäiltyjen haittavaikutusten epidemiologisen analysoinnin.
.png/27f530ad-4999-5939-9c11-57c8a1ee54a4?t=1672904202245&width=1500)
Fimean haittavaikutusrekisteriin tallennetaan Suomessa myyntiluvallisten lääkeaineiden haittavaikutusilmoitukset. Vuonna 2017 ilmoituksia tehtiin runsaat 3 000, joista noin viidennes koski rokotteita ja loput muita lääkkeitä. Aiemmin terveydenhuollon ammattilaiset velvoitettiin ilmoittamaan havaitsemastaan rokotteen haittavaikutusepäilystä. Uuden tartuntatautilain myötä ilmoittaminen on vapaaehtoista. Ilmoituksia voivat tehdä sekä terveydenhuollon ammattilaiset että kansalaiset.
Rokotteiden haittasignaaleja saadaan useista eri tiedonlähteistä
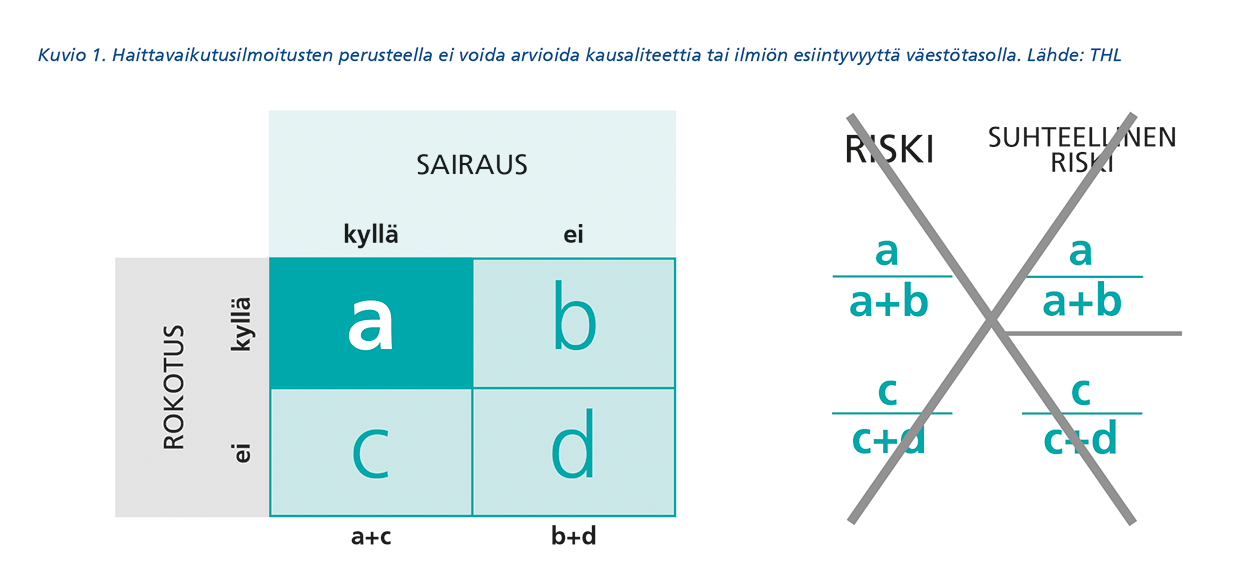
Fimean haittavaikutustietokannan tarkoituksena on toimia yhtenä tiedonlähteenä uusien odottamattomien haittasignaalien havaitsemiseksi. Koska haittavaikutusten raportointi on vapaaehtoista ja perustuu yksilöiden aktiivisuuteen, haittavaikutusrekisterin tietojen perusteella ei voida arvioida haitan esiintyvyyttä väestötasolla (kuvio 1). Rekisteri sisältää tiedot ainoastaan niistä altistuneista, joista haittavaikutusepäily on ilmoitettu.
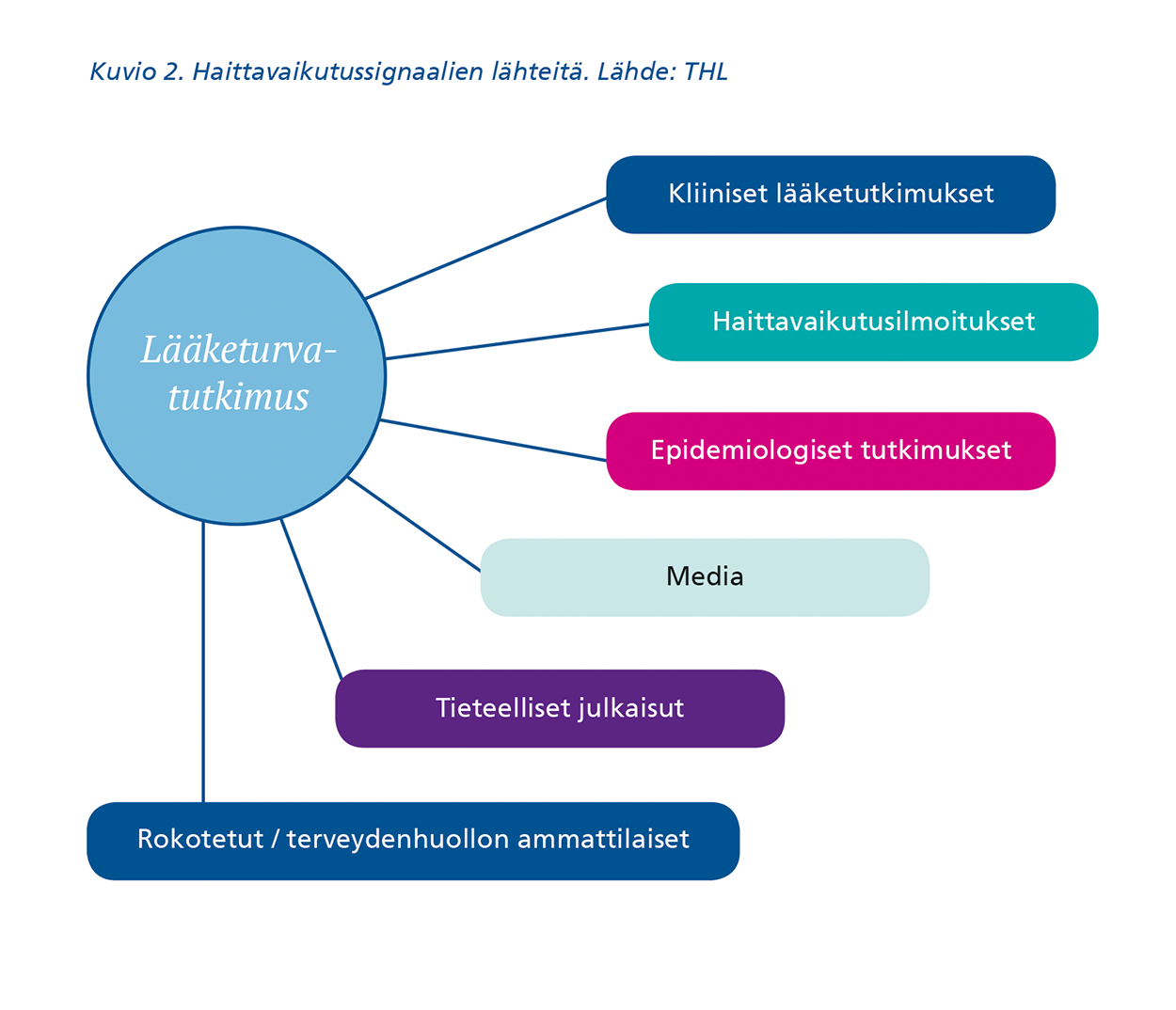
Mahdollisia haittasignaaleja voidaan havaita haittavaikutusrekisterin lisäksi esimerkiksi rokotetun omana havaintona, kliinisessä potilastyössä, mediasta, koe-asetelmaan perustuvissa tutkimuksissa, epidemiologisissa tutkimuksissa, tieteellisistä julkaisuista tai tiedonlouhinnan tuloksena (kuvio 2).
Rekisteriaineistot mahdollistavat rokotteiden haittasignaalien analysoinnin
THL:n ylläpitämän valtakunnallisen rokotusrekisterin avulla voidaan seurata rokotusten kattavuutta, tehoa ja turvallisuutta. Yhdistämällä sen sisältämiä tietoja valtakunnallisiin muihin terveysrekistereihin, saadaan luotettavaa tietoa rokotusten ja niiden epäiltyjen haittavaikutusten mahdollisesta yhteydestä.
Rokottaja kirjaa tiedot antamastaan rokotteesta sähköiseen potilastietojärjestelmään, josta ne siirtyvät valtakunnalliseen rokotusrekisteriin. Yhdistämällä henkilötiedot, rokotusrekisterin tiedot ja sairaaloiden hoitoilmoitusrekisterin tiedot, voidaan tarkistaa, onko kyseistä haittatapahtumaa esiintynyt enemmän kyseistä rokotetta saaneilla kuin rokottamattomilla. Tämä antaa viitteitä siitä, olisiko rokottamisen ja epäillyn haitan välillä ajallisen yhteyden lisäksi myös syy-seuraussuhde. Lisäksi saadaan taustatietoa, kun arvioidaan syysuhteen ajallisia muutoksia. Tavoitteena on, että rokotus- ja muiden terveysrekisterien tietoja käytettäisiin entistä enemmän epäiltyihin haittasignaaleihin liittyvien syysuhteiden selvittämiseen epidemiologisin keinoin (kuvio 3).
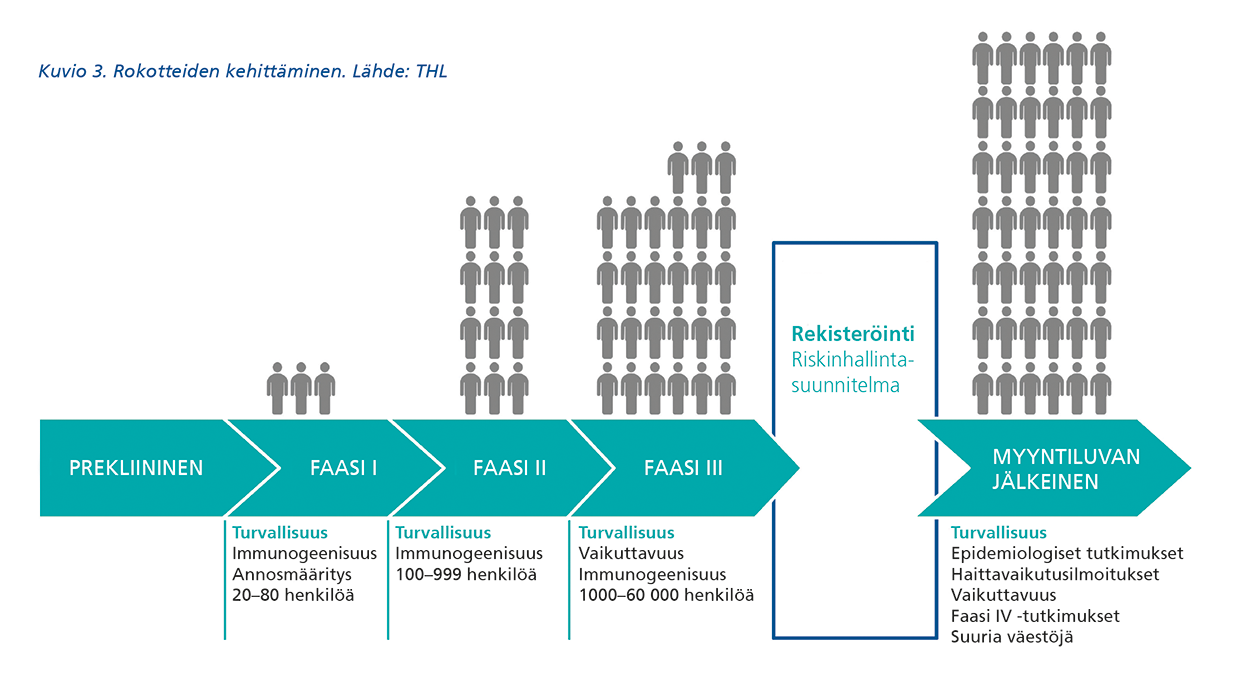
Valtakunnalliset terveysrekisterit tarjoavat mahdollisuuden arvioida ongelman laajuutta kattavasti väestötasolla. Valtakunnalliset terveysrekisterit on lähtökohtaisesti perustettu hallinnollisiin tarkoituksiin tai viranomaisseurantaan (esim. THL:n rokotusrekisteri, syntyneiden lasten rekisteri ja epämuodostumarekisteri) ei ensisijaisesti tutkimuksen tiedonlähteeksi. Rekisterit sisältävät kuitenkin laajasti tietoa, jota voidaan käyttää toissijaisesti myös tutkimuksen tekemiseen. Pelkästään rekisteritietoja käyttämällä saadaan muodostettua tutkimusaineisto, jonka avulla kausaliteetin arvioiminen sekä sekoittavien ja muiden tekijöiden huomioiminen on usein mahdollista. Lisäksi potilaskertomusten tietoja voidaan käyttää rekisteritietojen vahvistamiseen.
Rokotusrekisteriä on hyödynnetty esimerkiksi tilanteissa, joissa on epäilty Pandemrix-rokotteen myötävaikuttaneen narkolepsian puhkeamiseen ja rotavirusrokotteen aiheuttaneen suolentuppeumaa. Myös HPV-rokotteen turvallisuutta on selvitetty rekisteritietoihin perustuvalla tutkimuksella. Rekisteriaineistot ovat mahdollistaneet erilaisten tutkimusasetelmien ja menetelmien käytön, esimerkiksi kohortti- ja itsekontrolloidut tutkimusasetelmat (self-controlled case-series).
Rekisteritietoihin perustuvat väestötasoiset aineistot ovat usein laajoja ja muodostuvat suurista määristä tutkittavia henkilöitä. Siitä huolimatta harvinaisia sairauksia tutkittaessa ongelmaksi voi muodostua liian pienet tapausmäärät, jolloin kausaliteetin arvioiminen tilastollisin menetelmin ei ole mahdollista, vaikka otoksena olisi koko maan kattava populaatio. Tällöin tutkimuksen toistaminen pidemmällä seuranta-ajalla voi antaa mahdollisuuden ongelman laajuuden arviointiin, kun ajassa ilmaantuvien tapausten määrä kasvaa harvinaisissakin sairauksissa.
Pohjoismaiden terveysrekisterit ovat sisällöltään ja luokituksiltaan monilta osin yhdenmukaisia. Pohjoismaiset yhteistyötutkimukset ovat yksi mahdollisuus tutkittavien populaatioiden laajentamiseksi tietyissä tutkimusasetelmissa, esimerkiksi arvioitaessa rokotteiden tai lääkkeiden turvallisuutta, jolloin tutkittavien määrä voi koostua miljoonista henkilöistä. Tutkimuksen laajentaminen usean maan aineistoihin ei kuitenkaan välttämättä ratkaise pieniin tapausmääriin liittyvää ongelmaa, sillä erittäin harvinaisten sairauksien tapausmäärät voivat silti jäädä muutamiin kymmeniin tai jopa yksittäisiin tapauksiin. Näissäkin tapauksissa tutkimuksen myöhempi toistaminen laajemmalla tutkimusaineistolla voi mahdollistaa epäiltyjen syy-yhteyksien selvittämisen.
Kirjallisuutta
Jokinen J, ym. Pandemiarokotteen ja narkolepsian yhteys aikuisilla - Varmennettuihin rekisteritietoihin perustuva tutkimus 2013. Julkaisusarja Työpaperi 17/2013. Helsinki: Terveyden ja hyvinvoinnin laitos 2013.
Karonen T, Sommarberg L. Haittavaikutusilmoitukset vuonna 2017. Sic! 2018; 8(3): 37–40.
Kieler H, ym. Selective serotonin reuptake inhibitors during pregnancy and risk of persistent pulmonary hypertension in the newborn: population based cohort study from the five Nordic countries. Julkaistu verkossa 12.1.2012. www.bmj.com
Leino T, ym. Evaluation of the intussusception risk after pentavalent rotavirus vaccination in Finnish infants. Julkaistu verkossa 7.3.2016. www.plosone.org
Nohynek H, ym. AS03 adjuvanted AH1N1 vaccine associated with an abrupt increase in the incidence of childhood narcolepsy in Finland. Julkaistu verkossa 28.3.2012. www.plosone.org
Skufca J, ym. The association of adverse events with bivalent human papilloma virus vaccination: A nationwide register-based cohort study in Finland. Vaccine 2018 Sep 18; 36(39): 5926–33.


.png/27f530ad-4999-5939-9c11-57c8a1ee54a4?version=1.0&t=1672904202245&width=1200)